近日,真实生物科技有限公司(以下简称“真实生物”)再次向港交所递交主板上市申请,中金公司担任独家保荐人。作为曾凭借首款国产新冠口服药阿兹夫定批准上市而崭露头角的企业,其核心价值与成长潜力备受市场关注。

根据新的招股书可以看出,真实生物在巩固抗病毒领域优势的同时,正积极向抗肿瘤、心脑血管疾病领域拓展,瞄准未被满足的临床需求,构建起具有独特性、多元化的产品管线布局。
明星产品“阿兹夫定”
真实生物的明星产品阿兹夫定作为1.1类原创新药,在2022年7月获得国家药监局用于治疗COVID-19的附条件批准,成为国内在疫情防控期间获批上市的本土研发新冠口服药,展现了卓越的临床价值。
在当时进口药物价格高企的市场环境下,辉瑞Paxlovid每疗程需两千元左右。阿兹夫定纳入医保后,价格不到其十分之一,每疗程仅需175元,显著提升了药物可及性。
该产品于2023年被纳入国家医保目录,并完成2024年度续约。据招股书披露,目前其已累计销售超过1,000万瓶,覆盖了全国31个省份超过50,000家医疗终端。
据其招股书,产品安全性与有效性在真实世界数据中,被独立第三方发表的177篇论文证实。
目前该药逐步转型为常规治疗药物。在季节性呼吸道疾病感染高发期,凭借丰富的真实世界用药数据和医保覆盖优势,其在临床治疗中继续发挥重要价值,并可为真实生物持续贡献收入。
经过近年来的深入研究发现,阿兹夫定作为30年来少有的一款具备双重机制的高选择性核苷类药物,不但可通过抑制肿瘤细胞DNA合成,还可以透过免疫调节提高免疫力。
基于该双重作用机制,真实生物正在积极推进阿兹夫定治疗肿瘤的单药疗法研究,重点布局多发性骨髓瘤、淋巴瘤及急性白血病等血液肿瘤适应症。同时,真实生物还布局三种联合治疗肿瘤方案:包括阿兹夫定与抗PD-1联合治疗肝癌及结直肠癌,以及阿兹夫定与哆希替尼联合治疗非小细胞肺癌,阿兹夫定联合CTX治疗淋巴瘤。
招股书显示,阿兹夫定与抗PD-1联合方案的临床前研究展现显著疗效,在动物模型(syngeneic CT26 colon cancer model和syngeneic H22 liver cancer model)中都实现100%肿瘤完全消除,且停药后100天内无复发。在研究者发起的人体试验中,阿兹夫定联合奥希替尼对末线治疗失败(包括奥希替尼治疗进展的病例)的非小细胞肺癌患者实现100%疾病控制率;阿兹夫定联合PD1抑制剂及抗VEGFR类药物对结直肠癌末线治疗失败患者的疾病控制率达75%。基于以上积极进展,真实生物计划将提交阿兹夫定联合PD-1抑制剂对于结直肠癌、肝癌等适应症的临床试验申请,持续推进该创新疗法在实体瘤领域的开发。
深耕HIV治疗领域
招股书显示,阿兹夫定于2021年7月获批用于治疗HIV感染附条件批准上市。根据弗若斯特沙利文的资料,阿兹夫定是全球唯一一款用于治疗HIV的双靶点口服核苷药物,同时作为NRTI和Vif辅助蛋白抑制剂,其核心优势双靶点机制将有利于降低耐药风险,高效实现的低剂量优势可有效减少药物相互作用。
当前全球HIV药物市场面临耐药性与用药依从性低两大挑战。传统NRTI药物如拉米夫定,每日用药达300毫克。庞大的剂量严重影响患者长期治疗的意愿与持续性,同时这又将加剧耐药风险。根据世卫组织发布的《2021年度艾滋病毒耐药性报告》显示,在接受一线ART治疗后病毒载量超过1,000拷贝/毫升的患者中,有83.1%的患者对其方案中的NRTI产生耐药性。临床急需要高效和长效的艾滋病治疗药物。
目前,全球范围内已上市的长效HIV疗法均为注射制剂,仍需要与每日口服药一起服用。仍未能解决每日用药的依从性问题。真实生物正在研发另一款具有独创性的新型口服HIV候选药物CL-197已经开始二期临床试验。其最大的优势在于,在服药168小时后仍然保持有效药物浓度,有望实现每周一次给药的治疗方案,或将成为全球首款长效口服HIV治疗药物。
独创性癌症药物管线
在癌症治疗领域,真实生物布局了具有独创性的EGFR靶向候选药物哆希替尼,作为中国常见的肺癌类型,目前面临耐药性与脑转移两大治疗困境。
研究显示,60%的EGFR突变肺癌患者在初始诊断时即确诊脑转移。血脑屏障的天然阻隔因素,使得多数靶向药物难以有效穿透至脑部病灶,而恶性脑转移患者的平均存活期仅为6个月。同时,前两代 EGFR-TKI因耐药性突变导致疗效下降,严重影响患者长期治疗效果。哆希替尼的出现有望破解这两大难题。
体外试验及动物研究显示,与上一代治疗药物奥希替尼相比,哆希替尼有毒代谢物水平降低多达 80%,显著提升了用药安全性。更值得关注的是,临床前药代分布研究证实,哆希替尼在肺部及脑部组织中的原型药含量高于奥希替尼,具备更强的血脑屏障穿透能力,为肺癌脑转移治疗提供了独特优势。哆希替尼I期临床试结果也展现出显著疗效:240mg 剂量组中,1 例患者脑部非靶病灶完全消失,2 例患者达到部分缓解(PR),且左肺上叶、左侧胸膜等非靶病灶均实现消退。
目前哆希替尼已顺利进入II期临床试验,若未来成功上市,将为肺癌脑转移肿瘤的治疗提供新的选择。阿兹夫定与哆希替尼合并也将为现有耐药非小细胞肺癌患者提供更安全、有效的治疗选择。
除哆希替尼外,真实生物还布局了另一款颠覆性癌症管线——新型TOPO1抑制剂ZSSW-136,这可能是60年来第一个立体结构的非喜树碱环类抗肿瘤候选药物或毒素,可为TOPO1抑制剂临床用药提供新的治疗选择。
过往TOPO1抑制剂领域长期由喜树碱衍生物(如伊立替康、SN-38、DXd)主导,80%以上ADC药物采用同类毒素,但这类TOPO1抑制剂及其ADC药物在临床治疗半年到一年左右大多产生耐药,急需开发对这些耐药肿瘤有效的治疗药物。
ZSSW-136通过AI-CADD 技术打破传统母核结构限制,靶向TOPO1突变及药物外排泵,临床前研究中表现出对现有TOPO1抑制剂及其ADC耐药的肿瘤有显著疗效。在多个患者来源的伊立替康耐药肿瘤类人类器官实验中,显示出比伊立替康高400倍的活性。在伊立替康耐药肿瘤PDX动物模型上,ZSSW-136可以完全抑制肿瘤的生长。ZSSW-136类药物作为ADC毒素,可望为现有ADC耐药肿瘤提供有效的解决方案。推向一线治疗后,其治疗的无进展时期和总生存期或将显著延长,具有巨大的临床价值和经济价值。
ZSSW-136也展现出富有想象空间的商业化前景。据招股书披露,其应用场景十分灵活,既可以单独开发药物治疗实体肿瘤,也能作为“抗癌活性成分”,搭配 ADC(抗体偶联药物)、PDC(肽偶联药物)等常见的XDC类靶向药物使用,提升这类药物的疗效。目前真实生物已启动BD合作,有望通过“技术授权+里程碑付款”模式,助力下一代 XDC 药物研发,既助力解决行业内的耐药难题,也为公司预留了广阔商业空间。
明星科学家掌舵
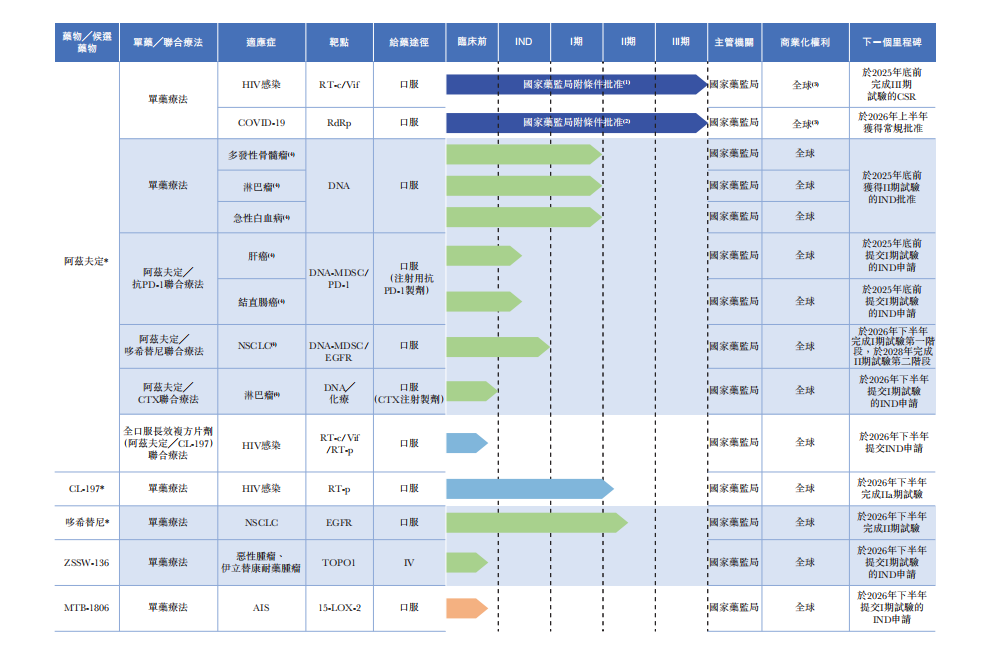
真实生物招股书中产品管线图
相较于上次递表,真实生物的多个研发管线取得了显著进展。这些成果的背后,可以看到以杜锦发博士为核心的科学家团队不懈努力的汗水。
作为公司董事长、首席执行官兼首席科学官杜锦发博士被认定为“国家特聘专家”,是丙肝治疗药物索非布韦的发明者之一。此药曾获得美国盖伦奖(被誉为医药界的诺贝尔奖),索非布韦治愈丙肝被《细胞》杂志誉为当代最重大的公共卫生成就之一。杜博士也是阿兹夫定(用于治疗COVID-19)、CL-197及哆希替尼的发明者之一。
在他的带领下,真实生物组建了一支具有跨国药企或顶尖科研机构工作背景的研发团队,核心成员平均拥有近30年行业经验,推动公司建立了包括高选择性核苷类抗肿瘤药物研发平台、新型TOPO1抑制剂及XDC药物研发平台等在内的综合研发体系。这些技术平台覆盖了从早期靶点发现到候选药物优化的全流程,不仅为当前管线的持续推进提供保障,也为未来持续产出创新药物奠定了坚实基础。
在当前中国医药创新政策持续利好、医疗需求不断升级的背景下,若真实生物此次赴港上市成功,将有望加速其多元化研发管线的推进。随着国家对创新药审评审批流程的持续优化,以及医保目录动态调整机制的不断完善,将推动创新药领域持续突破,为更多患者群体带来新的、更好的治疗选择。
(信息披露内容以公司公告为准。)